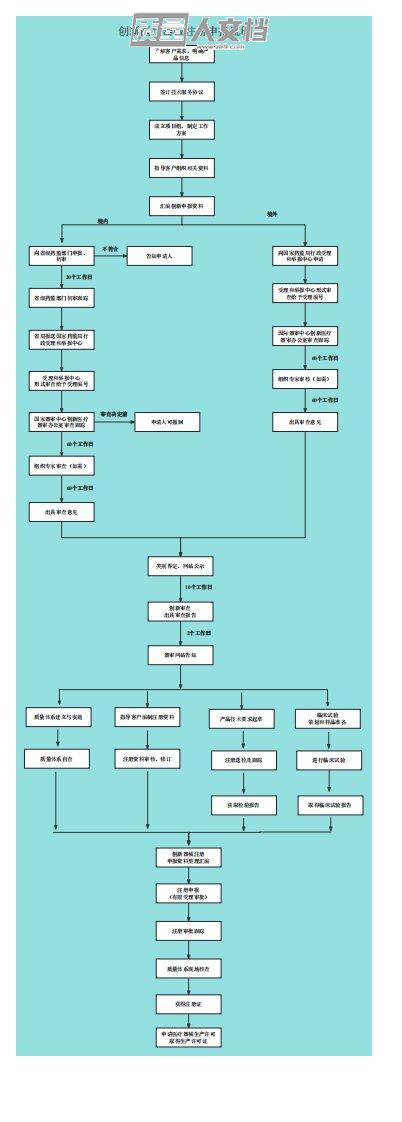
创新医疗器械注册申报流程
摘要:
展开>>
收起<<
创新医疗器械注册申报流程了解客户需求,明确产品信息签订技术服务协议成立项目组,制定工作方案指导客户组织相关资料汇编创新申报资料向省级药监部门申报、初审向国家药监局行政受理和举报中心申请境外境外省级药监部门初审跟踪受理和举报中心形式审查给予受理编号省局报送国家药监局行政受理和举报中心境内境内不符合不符合告知申请人受理和举报中心形式审查给予受理编号20个工作日个工作日国家器审中心创新医疗器审办公室审查跟踪申请人可撤回审查决定前审查决定前组织专家审查(如需)60个工作日个工作日60个工作日个工作日出具审查意见国际器审中心创新医疗器审办公室审查跟踪组织专家审核(如需)出具审查意见60个工作日个工作日6...
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
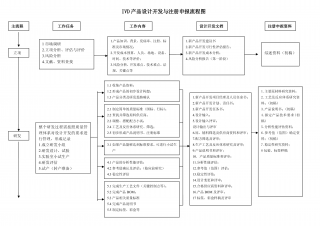
IVD产品设计开发以及注册申报流程图VIP免费
 2024-04-12 259
2024-04-12 259 -
医疗器械设计开发控制指南VIP免费

 2024-04-12 329
2024-04-12 329 -
YY∕T 0664-2020医疗器械软件软件生存周期过程核查表VIP免费

 2024-04-12 336
2024-04-12 336 -
创新医疗器械注册申报流程

 2024-05-02 171
2024-05-02 171 -
20221028_医疗器械生产现场核查缺陷分析交流(江苏药省监局审核查验中心) (1)VIP免费

 2024-05-09 123
2024-05-09 123 -
医疗器械网络安全漏洞自评报告VIP专享

 2024-11-18 343
2024-11-18 343 -
内审检查表 MDR法规VIP免费

 2025-04-07 314
2025-04-07 314 -
07.产品风险管理报告VIP免费

 2025-09-12 82
2025-09-12 82 -
06.可用性确认报告或可用性总结性测试报告VIP免费

 2025-09-12 124
2025-09-12 124 -
特定上市前提交审查的质量管理体系信息-2025草案_中英文版VIP专享

 2025-11-03 74
2025-11-03 74
作者: 51zlzl
分类:专业资料
价格:免费
属性:1 页
大小:47.51KB
格式:PDF
时间:2024-05-02


