可重复使用医疗器械的清洁验证过程-28页
VIP免费



标签: #可重复使用医疗器械 #清洁验证
摘要:
展开>>
收起<<
可重复使用医疗器械的清洗验证内容摘要有关背景要求和术语有关验证法规和指南FDA法规解读AAMITIR30解读模拟使用测试方案报告举例有关背景要求1、可重复使用医疗器械的设计要合理(便于用户进行方便和有效的清洁以及必要的消毒或灭菌)2、制造商应充分明确再处理的信息(证明再处理的信息已经过验证并易于用户理解且具有可操作性)。3、再处理过程通常包括清洁、消毒或灭菌(清洁用来去除污物,消毒或灭菌用以灭活微生物)。4、清洁是通过物理方式去除污物;所采用的清洁方法和试剂应能有效去除污物。清洁的效果将影响最终消毒和灭菌的效果,所以清洁步骤应单独进行验证。5、再处理说明都应包含每个清洁、冲洗、干燥...
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
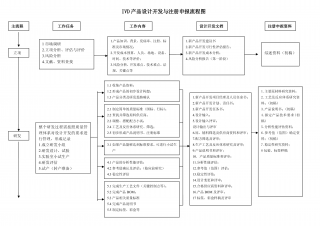
IVD产品设计开发以及注册申报流程图VIP免费
 2024-04-12 246
2024-04-12 246 -
医疗器械设计开发控制指南VIP免费

 2024-04-12 320
2024-04-12 320 -
YY∕T 0664-2020医疗器械软件软件生存周期过程核查表VIP免费

 2024-04-12 324
2024-04-12 324 -
创新医疗器械注册申报流程

 2024-05-02 168
2024-05-02 168 -
20221028_医疗器械生产现场核查缺陷分析交流(江苏药省监局审核查验中心) (1)VIP免费

 2024-05-09 120
2024-05-09 120 -
医疗器械网络安全漏洞自评报告VIP专享

 2024-11-18 341
2024-11-18 341 -
内审检查表 MDR法规VIP免费

 2025-04-07 309
2025-04-07 309 -
07.产品风险管理报告VIP免费

 2025-09-12 78
2025-09-12 78 -
06.可用性确认报告或可用性总结性测试报告VIP免费

 2025-09-12 121
2025-09-12 121 -
特定上市前提交审查的质量管理体系信息-2025草案_中英文版VIP专享

 2025-11-03 71
2025-11-03 71
作者:宁静致远
分类:培训考试
价格:60质量币
属性:28 页
大小:801.31KB
格式:PDF
时间:2024-11-16


