医疗器械注册质量体系核查的程序和检查
摘要:
展开>>
收起<<
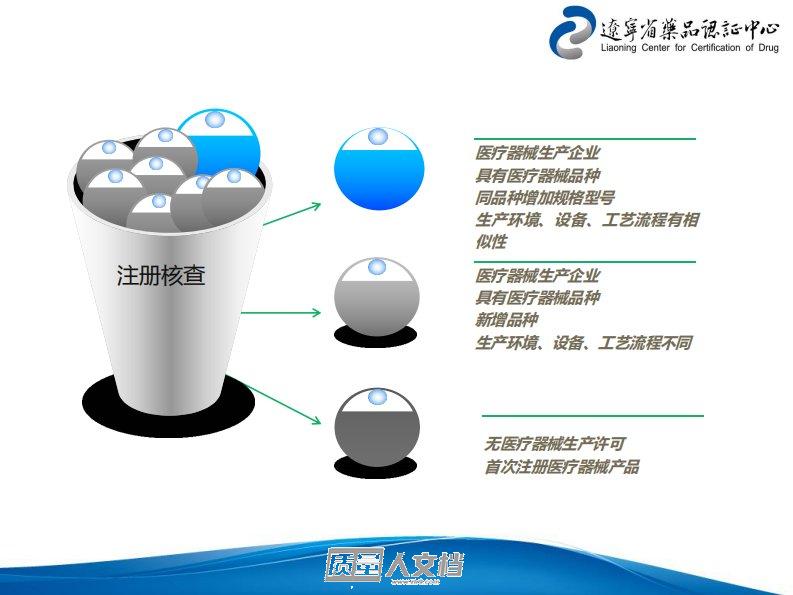
辽宁省医疗器械注册质量体系核查检查要求目的1.判断研制和样品生产过程是否按规范进行2.是否在体系内受控3.判断研制过程是否真实4.判断样品是否真实生产5.判断企业是否具备生产能力(厂房、设施设备、工艺、SOP)6.申报资料关键内容是否与设计输出一致医疗器械生产企业具有医疗器械品种同品种增加规格型号生产环境、设备、工艺流程有相似性医疗器械生产企业具有医疗器械品种新增品种生产环境、设备、工艺流程不同无医疗器械生产许可首次注册医疗器械产品注册核查1•62家企业•101个品种•331条缺陷项(48条主要缺陷)注册核查主要存在的问题17.2.1应当编制生产工艺规程、作业指导书等,明确关键工序和特殊过程。...
相关推荐
-
GB∕T 16886.12-2023 医疗器械生物学评价 第12部分:样品制备与参照材料VIP免费

 2024-04-14 46
2024-04-14 46 -
GB∕T 14233.1-2022 医用输液、输血、注射器具检验方法 第1部分:化学分析方法

 2024-04-16 85
2024-04-16 85 -
GB∕T 2828.3-2008 计数抽样检验程序 第3部分:跳批抽样程序

 2024-04-17 22
2024-04-17 22 -
GB∕T 25915.2-2021 洁净室及相关受控环境 第2部分:洁净室空气粒子浓度的监测

 2024-04-17 72
2024-04-17 72 -
GB∕T 19973.1-2023 医疗保健产品灭菌 微生物学方法 第1部分:产品上微生物总数的确定

 2024-04-18 25
2024-04-18 25 -
GB 2761-2017 食品安全国家标准 食品中真菌毒素限量VIP免费

 2024-04-19 21
2024-04-19 21 -
GB∕Z 42217-2022 医疗器械 用于医疗器械 质量体系软件的确认VIP免费

 2024-04-19 33
2024-04-19 33 -
GB∕T 42125.10-2022测量、控制和实验室用电气设备的安全要求 第10部分:绝缘电阻测量和介电强度试验设备的特殊要求VIP免费

 2024-04-19 24
2024-04-19 24 -
GB∕T 42062-2022 医疗器械 风险管理对医疗器械的应用VIP免费

 2024-04-19 46
2024-04-19 46 -
GB∕T 35770-2022 合规管理体系 要求及使用指南VIP免费

 2024-04-19 57
2024-04-19 57
作者:宁静致远
分类:培训考试
属性:30 页
大小:783.79KB
格式:PDF
时间:2024-05-20