3.《北京市医疗器械灭菌工艺检查要点指南(2023版)》(征求意见稿)
《北京市医疗器械灭菌工艺
检查要点指南(2023 版) 》修订说明
为了贯彻落实《医疗器械生产质量管理规范》及相关配
套文件要求,加强北京市医疗器械生产科学监管,指导和规
范北京市医疗器械生产企业监督检查工作,帮助检查人员增
强对医疗器械灭菌工艺的认识,明确对企业医疗器械灭菌工
艺的基本要求,北京市药监局结合相关法规及标准变化情
况, 以及北京市监管工作实际,组织对《医疗器械灭菌工
艺 检查要点指南(2010 版)》进行了修订。
一、修订背景
原北京市药品监督管理局组织编制了《医疗器械灭菌工艺
检查要点指南(2010 版)》, 旨在帮助北京市医疗器械监
管 人员对医疗器械灭菌工艺的熟悉和掌握,指导全市医疗器
械监 管人员对相关企业开展监督检查,同时,为医疗器械生
产企业 开展相关生产管理活动提供参考。
为进一步落实新版医疗器械生产监管法规和相关标准
要求,我局于今年组织开展对《医疗器械灭菌工艺检查要点
指南 ( 2010 版) 》 进 行了 修 订 ,结合 相 关法规 及 标准变
化, 以及本市医疗器械监管人员的监管实践,进一步指导
相关医 疗器械生产企业做好医疗器械灭菌工艺检查工作。
二、修订思路
结合相关法规、标准要求的变化,以及北京市医疗器械灭
菌工艺监管实际,对原指南有关内容进一步修改完善,有效落
1
实医疗器械法规、标准要求,对北京市医疗器械灭菌工艺相关
监管工作进行科学指导,全力提升科学监管工作水平。
三、主要修订内容
此次修订,主要对以下内容进行了修改和完善:
( 一)为强化对实际监管工作的指导性,结合新法规
新 标准变化和监管工作实际,加入对注册人、备案人和受
托生 产企业的有关要求等。
( 二)结合生产企业常用的灭菌方法,对灭菌工艺的
监 督检查进行了完善,新增了湿热灭菌的检查内容,为生
产企 业的灭菌工艺过程管理提供参考和依据。
( 三)将原指南中引用的法规、标准及有关文件按照
现 行版本进行了更新。
2
北京市医疗器械灭菌工艺检查要点
指南(2023 版)
(征求意见稿)
灭菌工艺过程控制是无菌医疗器械生产企业质量管理
体系中极其重要的一环,灭菌控制水平的结果直接影响着无
菌医疗器械产品的质量安全。为加强对医疗器械灭菌工艺的
管理及相关监督检查,进一步贯彻国家药品监督管理局关于
《医疗器械生产质量管理规范》实施的具体要求,依据《医
疗器械生产质量管理规范》及相关配套文件,制定本指南。
本指南旨在帮助北京市医疗器械生产监管人员增强对
无菌医疗器械相关知识的认识,指导和规范全市医疗器械生
产监管人员对医疗器械注册人、备案人、受托生产企业(
以 下简称 “生产企业”)灭菌工艺控制水平的监督检查工
作,
同时,为生产企业的灭菌工艺过程管理要求提供参考和依据。
本指南中引用的国家相关法规、规章、标准、检查指南
等版本发生变化时,要以执行的最新版为准。必要时,北京
市药品监督管理局应重新研究修订, 以确保本指南持续符
合 要求。
一、适用范围
根据灭菌方式的不同,医疗器械行业常用的灭菌方法有
环氧乙烷灭菌( 以下简称 EO 灭菌)、辐射灭菌和湿热灭
菌 等。本指南主要用于对目前北京市生产企业普遍采用的
EO 灭菌、钴-60(60Co)辐射灭菌和湿热灭菌的监督检查。
3
摘要:
展开>>
收起<<
《北京市医疗器械灭菌工艺检查要点指南(2023版)》修订说明为了贯彻落实《医疗器械生产质量管理规范》及相关配套文件要求,加强北京市医疗器械生产科学监管,指导和规范北京市医疗器械生产企业监督检查工作,帮助检查人员增强对医疗器械灭菌工艺的认识,明确对企业医疗器械灭菌工艺的基本要求,北京市药监局结合相关法规及标准变化情况,以及北京市监管工作实际,组织对《医疗器械灭菌工艺检查要点指南(2010版)》进行了修订。一、修订背景原北京市药品监督管理局组织编制了《医疗器械灭菌工艺检查要点指南(2010版)》,旨在帮助北京市医疗器械监管人员对医疗器械灭菌工艺的熟悉和掌握,指导全市医疗器械监管人员对相关企业开展监...
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
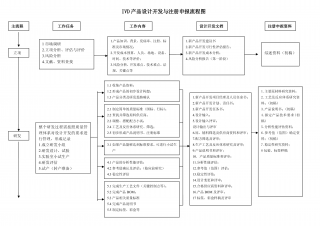
IVD产品设计开发以及注册申报流程图VIP免费
 2024-04-12 148
2024-04-12 148 -
医疗器械设计开发控制指南VIP免费

 2024-04-12 220
2024-04-12 220 -
YY∕T 0664-2020医疗器械软件软件生存周期过程核查表VIP免费

 2024-04-12 202
2024-04-12 202 -
创新医疗器械注册申报流程

 2024-05-02 110
2024-05-02 110 -
20221028_医疗器械生产现场核查缺陷分析交流(江苏药省监局审核查验中心) (1)VIP免费

 2024-05-09 73
2024-05-09 73 -
医疗器械网络安全漏洞自评报告VIP专享

 2024-11-18 263
2024-11-18 263 -
内审检查表 MDR法规VIP免费

 2025-04-07 157
2025-04-07 157 -
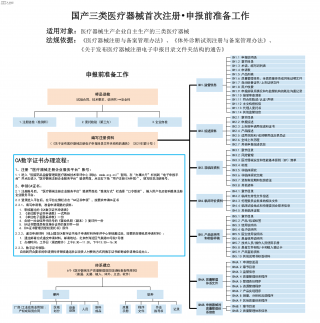
国产三类医疗器械首次注册-申报前准备工作VIP免费
 2025-09-03 19
2025-09-03 19 -
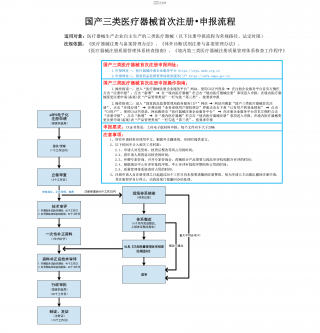
国产三类医疗器械首次注册-申报流程VIP免费
 2025-09-03 23
2025-09-03 23 -
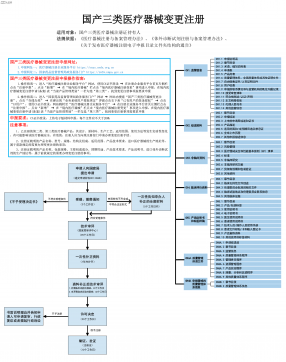
国产三类医疗器械变更注册VIP免费
 2025-09-03 18
2025-09-03 18
作者:多多猪
分类:专业资料
属性:35 页
大小:78.1KB
格式:DOCX
时间:2025-07-26


