6.《北京市医疗器械无菌试验检查要点指南(2023版)》(征求意见稿)
《北京市医疗器械无菌试验
检查要点指南(2023 版) 》修订说明
为了贯彻落实《医疗器械生产质量管理规范》及相关配套文件
要求,加强北京市医疗器械生产科学监管,指导和规范北京市医疗
器械生产企业监督检查工作,帮助检查人员增强对医疗器械无菌试
验的认识,明确对企业医疗器械无菌试验的基本要求,北京市药监
局结合相关法规及标准变化情况,以及北京市监管工作实际,组织
对《医疗器械无菌试验检查要点指南》(2010 版)进行了修订。
一、修订背景
医疗器械无菌检验主要依据为《中华人民共和国药典》( 以
下 简称“药典”),药典现行有效版本为 2020 版,其中无菌检验相
关内 容较 2010 版有较大差异,为与药典内容保持一致,同时参
照相关 管理规范和国行标的要求,修订原有文件。
二、修订思路
结合相关法规、标准要求的变化, 以及北京市医疗器械无菌
试 验监管实际,对原指南有关内容进一步修改完善,有效落实医
疗器 械法规、标准要求,对北京市医疗器械无菌试验相关监管工
作进行 科学指导,全力提升科学监管工作水平。
三、主要修订内容
此次修订,主要对以下内容进行了修改和完善:
( 一)无菌检查有关要求
1
根据相关标准,将无菌检查环境洁净度要求由“10000
级下的
局部洁净度 100 级的单向流空气区域”修改为 “ 隔离器系统或
B 级背景下的 A 级单向流洁净区域”;阳性对照管培养时间
由“48~72 小时”修改为 “不超过 5 天”。
( 二 )涉及培养基有关要求
根据相关标准要求,针对培养基的种类、保存期、培养基制
备及适用性检查要求进行了修订。如对培养基种类由 “ 改良马丁
培 养基”修改为 “胰酪大豆胨液体培养基”;对制备好的培养基
增加 了需进行保存期验证的要求;删除了改良马丁培养基、营养
肉汤培 养基、营养琼脂培养基的配制方法,增加了胰酪大豆胨液体
培养基、 胰酪大豆胨液体琼脂培养基、沙氏葡萄液体培养基和沙
氏葡萄糖琼 脂培养基等的配制方法;硫乙醇酸盐流体培养基的接菌
种类由 “金 黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌和生孢
梭菌”修改为 “金黄色葡萄球菌、铜绿假单胞菌和生孢梭菌”;
胰酪大豆胨液体 培养基(替代 “ 改良马丁培养基” )的接菌种
类由 “ 白色念珠菌和 黑曲霉”修改为 “枯草芽孢杆菌、 白色念
珠菌和黑曲霉”等等。
( 三)无菌试验培养及观察
试验观察要求由 “逐日观察”修改为 “定期观察”;对培
养 基出现浑浊后的后续转种要求做了修改;对培养基制备记录
增加 了需记录灭菌后培养基 pH 值的要求;无菌试验原始记录中
增加了 需记录所使用培养基批号的要求等。
( 四)方法适用性试验
2
硫乙醇酸盐流体培养基的接菌种类由 “金黄色葡萄球菌、大
肠埃希菌、枯草芽孢杆菌和生孢梭菌”修改为“金黄色葡萄球菌、
大肠埃希菌和生孢梭菌”;胰酪大豆胨液体培养基(替代 “ 改良
马丁培养基”)的接菌种类由“ 白色念珠菌和黑曲霉”修改为“枯
草芽孢杆菌、 白色念珠菌和黑曲霉”。
( 五)供试品相关要求
供试品数量由“应满足同一批号 3~ 11 个单位供试品”修改为
“应满足标准中对于检验样品数量的要求”, 以满足国标修订的
要求;检验量的定义由 “一次试验所用 的 供试品 总 量
(g/mL)” 修改为 “供试品每个最小包装接种至每份培养基的
最小量”;按 照 2020 版药典重新修订了 “表 1 批出厂产品最
少量检验数量” 、 “表 2 上市抽验样品的最少检验数量”和
“表 3 供试品的最少检 验量” 的内容。
( 六)名词解释
根据最新管理规范和国标要求,对常见的名词解释内容进行
了修订,并对正文中涉及到的关键术语增加了相应名词解释。
3
摘要:
展开>>
收起<<
《北京市医疗器械无菌试验检查要点指南(2023版)》修订说明为了贯彻落实《医疗器械生产质量管理规范》及相关配套文件要求,加强北京市医疗器械生产科学监管,指导和规范北京市医疗器械生产企业监督检查工作,帮助检查人员增强对医疗器械无菌试验的认识,明确对企业医疗器械无菌试验的基本要求,北京市药监局结合相关法规及标准变化情况,以及北京市监管工作实际,组织对《医疗器械无菌试验检查要点指南》(2010版)进行了修订。一、修订背景医疗器械无菌检验主要依据为《中华人民共和国药典》(以下简称“药典”),药典现行有效版本为2020版,其中无菌检验相关内容较2010版有较大差异,为与药典内容保持一致,同时参照相关管理...
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
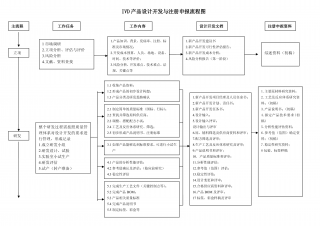
IVD产品设计开发以及注册申报流程图VIP免费
 2024-04-12 148
2024-04-12 148 -
医疗器械设计开发控制指南VIP免费

 2024-04-12 220
2024-04-12 220 -
YY∕T 0664-2020医疗器械软件软件生存周期过程核查表VIP免费

 2024-04-12 202
2024-04-12 202 -
创新医疗器械注册申报流程

 2024-05-02 110
2024-05-02 110 -
20221028_医疗器械生产现场核查缺陷分析交流(江苏药省监局审核查验中心) (1)VIP免费

 2024-05-09 73
2024-05-09 73 -
医疗器械网络安全漏洞自评报告VIP专享

 2024-11-18 263
2024-11-18 263 -
内审检查表 MDR法规VIP免费

 2025-04-07 157
2025-04-07 157 -
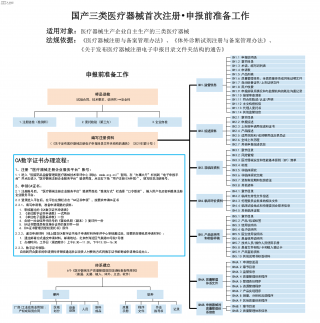
国产三类医疗器械首次注册-申报前准备工作VIP免费
 2025-09-03 19
2025-09-03 19 -
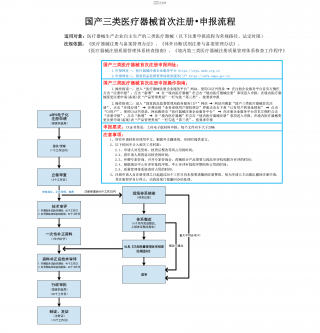
国产三类医疗器械首次注册-申报流程VIP免费
 2025-09-03 23
2025-09-03 23 -
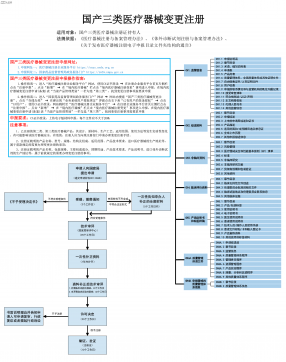
国产三类医疗器械变更注册VIP免费
 2025-09-03 18
2025-09-03 18
作者:多多猪
分类:专业资料
属性:29 页
大小:57.65KB
格式:DOCX
时间:2025-07-26


