浅谈如何开展医疗器械同品种临床评价-71页
VIP免费
浅谈如何开展
医疗械器械同品种临床评价
一、简述医疗器械临床评价
二、怎样选择同品种
三、如何开展等同性论证
四、同品种支持性资料准备
五、同品种临床数据分析
内
容
一、简述医疗器械临床评价
Ø法规依据: 《医疗器械监督管理条例》
第二十五条 进行医疗器械临床评价,可以根据产品设计特征、临床风险、
已有临床数据等情形,通过开展临床试验,或者通过对同品种医疗器械临床文献
资料、临床数据进行分析评价,证明医疗器械安全、有效。
解读:分层次的临床评价要求,与具体产品的安全有效性评价相适应,且
临床评价目标明确、重点突出,有利于严守安全有效底线。
摘要:
展开>>
收起<<
浅谈如何开展医疗械器械同品种临床评价一、简述医疗器械临床评价二、怎样选择同品种三、如何开展等同性论证四、同品种支持性资料准备五、同品种临床数据分析内容一、简述医疗器械临床评价Ø法规依据:《医疗器械监督管理条例》 第二十五条进行医疗器械临床评价,可以根据产品设计特征、临床风险、已有临床数据等情形,通过开展临床试验,或者通过对同品种医疗器械临床文献资料、临床数据进行分析评价,证明医疗器械安全、有效。解读:分层次的临床评价要求,与具体产品的安全有效性评价相适应,且临床评价目标明确、重点突出,有利于严守安全有效底线。一、简述医疗器械临床评价Ø法规依据:《医疗器械监督管理条例》 第二十四条 医疗器械产品...
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
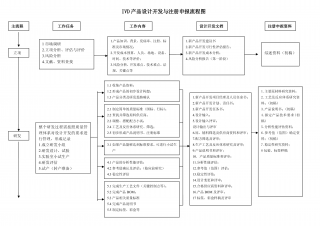
IVD产品设计开发以及注册申报流程图VIP免费
 2024-04-12 148
2024-04-12 148 -
医疗器械设计开发控制指南VIP免费

 2024-04-12 220
2024-04-12 220 -
YY∕T 0664-2020医疗器械软件软件生存周期过程核查表VIP免费

 2024-04-12 202
2024-04-12 202 -
创新医疗器械注册申报流程

 2024-05-02 110
2024-05-02 110 -
20221028_医疗器械生产现场核查缺陷分析交流(江苏药省监局审核查验中心) (1)VIP免费

 2024-05-09 73
2024-05-09 73 -
医疗器械网络安全漏洞自评报告VIP专享

 2024-11-18 263
2024-11-18 263 -
内审检查表 MDR法规VIP免费

 2025-04-07 157
2025-04-07 157 -
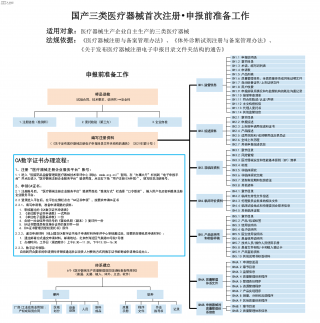
国产三类医疗器械首次注册-申报前准备工作VIP免费
 2025-09-03 19
2025-09-03 19 -
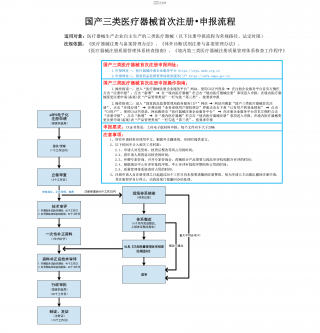
国产三类医疗器械首次注册-申报流程VIP免费
 2025-09-03 23
2025-09-03 23 -
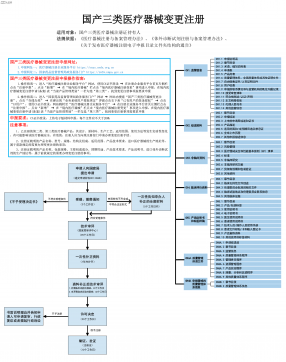
国产三类医疗器械变更注册VIP免费
 2025-09-03 18
2025-09-03 18
作者:多多猪
分类:专业资料
属性:71 页
大小:619.29KB
格式:PDF
时间:2025-08-29


