ISO13485程序文件(29份)
VIP免费


摘要:
展开>>
收起<<
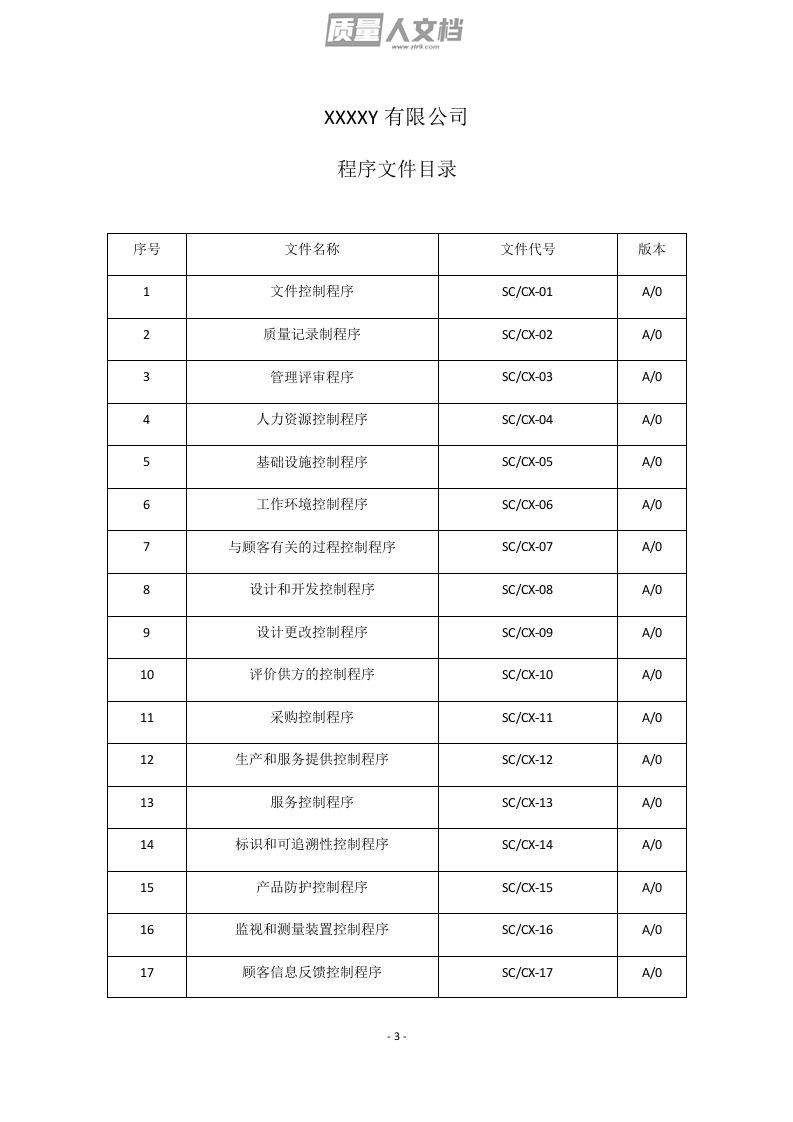
文件编号:SC/CX-A/0-2020控制状态:受控□非受控□版本号:A/0发放编号:SC-2020-001程序文件编制/日期:20XX年X月X日审核/日期:批准/日期:XXXXY有限公司20XX年X月X日发布20XX年X月X日实施XXXXY有限公司程序文件目录XXXXY有限公司程序文件目录1目的对与组织质量管理体系有关的文件进行控制,确保各相关场所使用文件均为有效版本。2范围文件的编制、评审、批准、发放、使用、更改、标识、回收和作废等全过程活动的管理。3职责3.1企业负责人负责批准发布《质量手册》、《程序文件》。3.2管理者代表负责审核《质量手册》、《程序文件》,对操作规范、检验文件、技术文...
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
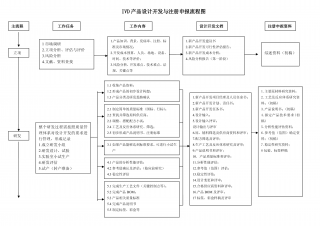
IVD产品设计开发以及注册申报流程图VIP免费
 2024-04-12 148
2024-04-12 148 -
医疗器械设计开发控制指南VIP免费

 2024-04-12 220
2024-04-12 220 -
YY∕T 0664-2020医疗器械软件软件生存周期过程核查表VIP免费

 2024-04-12 202
2024-04-12 202 -
创新医疗器械注册申报流程

 2024-05-02 110
2024-05-02 110 -
20221028_医疗器械生产现场核查缺陷分析交流(江苏药省监局审核查验中心) (1)VIP免费

 2024-05-09 73
2024-05-09 73 -
医疗器械网络安全漏洞自评报告VIP专享

 2024-11-18 263
2024-11-18 263 -
内审检查表 MDR法规VIP免费

 2025-04-07 157
2025-04-07 157 -
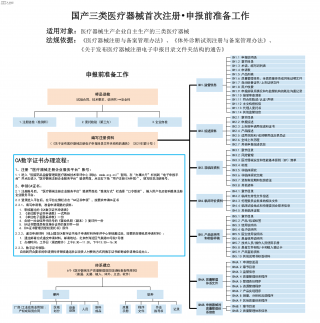
国产三类医疗器械首次注册-申报前准备工作VIP免费
 2025-09-03 19
2025-09-03 19 -
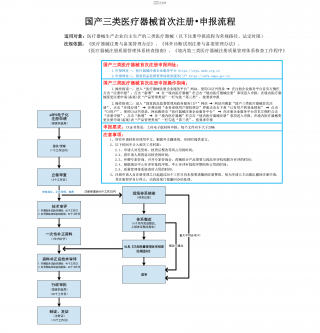
国产三类医疗器械首次注册-申报流程VIP免费
 2025-09-03 23
2025-09-03 23 -
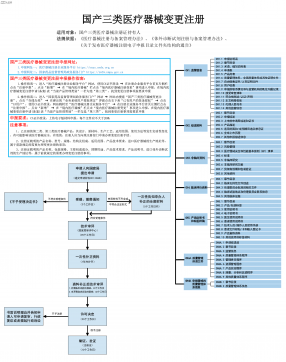
国产三类医疗器械变更注册VIP免费
 2025-09-03 18
2025-09-03 18
作者:盛夏阳光
分类:专业资料
属性:101 页
大小:269.1KB
格式:DOCX
时间:2025-05-23


