医疗器械生产企业法规考试试题题库(答案解析)-75页
VIP免费
序号 题型 题干 选项 答案
1 单选题 国家对医疗器械按照()实行分类管理。
A.预期目的
B.风险程度
C.有源与否
D.使用方法
B
2 单选题 ()应当经国务院药品监督管理部门批准。
A.第三类医疗器械临床试验
B.第三类医疗器械临床试验对人体具有较高风险
的
C.对人体具有较高风险的医疗器械临床试验
D.第二类、第三类医疗器械临床试验
B
3 单选题 医疗器械应当使用(),该名称应当符合国务院药
品监督管理部门制定的医疗器械命名规则。
A.专业名称
B.规范名称
C.正规名称
D.通用名称
D
4 单选题
医疗器械的生产条件发生变化,不再符合医疗器
械质量管理体系要求,可能影响医疗器械安全、
有效的,医疗器械注册人、备案人、受托生产企
业应当立即(),并向原生产许可或者生产备案部
门报告。
A.停止生产活动B.进行整改
C.进行内审D.采取相应安全措施 A
5 单选题 ()依法对进口的医疗器械实施检验;检验不合格
的,不得进口。
A.市场监督管理局B.医疗器械监督管理部门
C.药品监督管理部门D.出入境检验检疫机构 D
6 单选题 我国对()医疗器械实行产品备案管理。
A.第一类
B.第二类
C.第三类
D.第四类
A
7 单选题
医疗器械生产企业应当加强对工艺用水质量的管
理,确保工艺用水的()不对医疗器械产品质量造
成影响。
A.制备
B.使用
C.检验
D.制备和使用
D
8 单选题 应当确定工艺用水取样点,制定取样点分布图,
至少应当包括()个
A.1
B.2
C.3
D.4
C
9 单选题
1.药品医疗器械飞行检查,是指食品药品监督管
理部门针对药品和医疗器械研制、()、经营、
使用等环节开展的不预先告知的监督检查。
A.采购
B.质量
C.设计
D.生产
D
10 单选题
食品药品监督管理部门派出的检查组应当由()名
以上检查人员组成,检查组实行组长负责制。检
查人员应当是食品药品行政执法人员、依法取得
检查员资格的人员或者取得本次检查授权的其他
人员;根据检查工作需要,食品药品监督管理部
门可以请相关领域专家参加检查工作。
A.1
B.2
C.3
D.4
B
11 单选题
飞行检查发现的违法行为涉嫌犯罪的,由负责立
案查处的食品药品监督管理部门移送(),并抄
送同级检察机关。
A.公安机关;
B.法院;
C.市场监管部门;
D.卫生监管部门。
A
12 单选题
医疗器械上市许可持有人、经营企业、使用单位
应当建立并保存医疗器械不良事件监测记录。记
录应当保存至医疗器械有效期后()年;无有效
期的,保存期限不得少于()年。植入性医疗器
械的监测记录应当(),医疗机构应当按照病例
相关规定保存。
A.1、2、4
B.2、5、10
C.2、5、永久保存
D.2.10.10
C
13 单选题
医疗器械上市许可持有人发现或者获知可疑医疗
器械不良事件的,应当立即调查原因,导致死亡
的应当在()日内报告;导致严重伤害、可能导
致严重伤害或者死亡的应当在()日内报告。
A.5,10
B.5,15
C.7,10
D.7,20
D
14 单选题
3.医疗器械上市许可持有人在报告医疗器械不良
事件后或者通过国家医疗器械不良事件监测信息
系统获知相关医疗器械不良事件后,应当按要求
开展后续调查、分析和评价,导致死亡的事件应
当在()日内,导致严重伤害、可能导致严重伤
害或者死亡的事件应当在()日内向持有人所在
地省级监测机构报告评价结果。对于事件情况和
评价结果有新的发现或者认知的,应当补充报告
A.20,30
B.30,45
C.30,60
D.45,60
B
15 单选题
医疗器械生产企业连续停产()年以上且无同类
产品在产的,重新生产时,应当进行必要的验证
和确认,并书面报告药品监督管理部门。可能影
响质量安全的,药品监督管理部门可以根据需要
组织核查。
A、1;
B、2;
C、3;
D、4。
A
16 单选题 对生产重点监管产品目录品种的企业每年至少检
查()次。
A、1;
B、2;
C、3;
D、4。
A
17 单选题
企业应当建立健全管理者代表相关管理制度和考
核机制,为管理者代表履行职责提供必要条件,
同时确保其在履行职责时不受企业内部因素的不
当干扰。对于不能有效履职的管理者代表,企业
负责人应当立即代其履职,或者指定符合本规定
第六条要求的人员代其履行管理者代表职责,并
于()个工作日内确定和任命新的管理者代表。
A、10;
B、20;
C、30;
D、40。
C
18 单选题
生产企业负责人应当与管理者代表签订授权书,
明确管理者代表应当履行的质量管理职责并授予
相应的权限。企业应当在确定管理者代表()个
工作日内向所在地药品监督管理部门报告。
A、10;
B、15;
C、30;
D、40。
B
19 单选题
生产企业负责人应当每()至少听取一次管理者
代表工作情况汇报,对企业生产情况和质量安全
管理情况进行回顾分析,对风险防控重点工作进
行研究并作出调度安排,形成调度记录。
A、月;
B、季度;
C、半年;
D、年。
B
20 单选题
江苏省医疗器械生产分级监管实施办法中,()
负责确定本行政区域内第二、三类医疗器械生产
企业监管等级并实施监管。
A、省局各检查分局
B、省中心各分中心
C、设区市市场监督管理局
D、各地区综合执法局
A
21 单选题
江苏省医疗器械生产分级监管实施办法中,对实
施四级监管的企业,负责日常监管的药品监督管
理部门每年至少组织()次全项目检查。
A、1
B、2
C、3
D、4
A
22 单选题
江苏省医疗器械生产分级监管实施办法中,对实
施三级监管的企业,负责日常监管的药品监督管
理部门每年至少组织()次检查,其中每两年全
项目检查不少于()次。
A、1,2
B、2,1
C、1,1
D、2,2
C
23 单选题
江苏省医疗器械生产分级监管实施办法中,对实
施二级监管的企业,负责日常监管的药品监督管
理部门每两年检查不少于()次。
A、1
B、2
C、3
D、4
A
24 单选题
江苏省医疗器械生产分级监管实施办法中,对风
险程度较高的企业实施(),主要包括生产省局
《目录》内三级监管医疗器械的企业,未列入四
级监管的所有第三类医疗器械生产企业,以及质
量管理体系运行状况较差、有不良监管信用记录
的企业。
A、一级监管
B、二级监管
C、三级监管
D、四级监管
C
25 单选题 国家药监局关于发布禁止委托生产医疗器械目录
的主要目的是什么?
A、防止医疗器械生产企业之间的不正当竞争
B、为加强医疗器械生产监管,保障医疗器械安全
、有效
C、防止医疗器械产品的价格垄断
D、促进医疗器械行业的创新和发展
B
26 单选题
江苏省医疗器械生产分级监管实施办法中,对医
疗器械注册人备案人、受托生产企业的监管分为
()个级别。
A、一
B、二
C、三
D、四
D
摘要:
展开>>
收起<<
序号题型题干选项答案1单选题国家对医疗器械按照()实行分类管理。A.预期目的B.风险程度C.有源与否D.使用方法B2单选题()应当经国务院药品监督管理部门批准。A.第三类医疗器械临床试验B.第三类医疗器械临床试验对人体具有较高风险的C.对人体具有较高风险的医疗器械临床试验D.第二类、第三类医疗器械临床试验B3单选题医疗器械应当使用(),该名称应当符合国务院药品监督管理部门制定的医疗器械命名规则。A.专业名称B.规范名称C.正规名称D.通用名称D4单选题医疗器械的生产条件发生变化,不再符合医疗器械质量管理体系要求,可能影响医疗器械安全、有效的,医疗器械注册人、备案人、受托生产企业应当立即(),并...
声明:如果您的权利被侵害,请联系我们的进行举报。
相关推荐
-
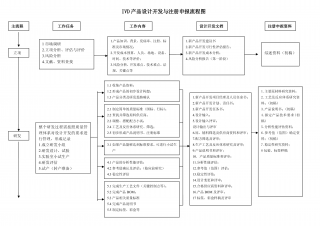
IVD产品设计开发以及注册申报流程图VIP免费
 2024-04-12 140
2024-04-12 140 -
医疗器械设计开发控制指南VIP免费

 2024-04-12 216
2024-04-12 216 -
YY∕T 0664-2020医疗器械软件软件生存周期过程核查表VIP免费

 2024-04-12 196
2024-04-12 196 -
创新医疗器械注册申报流程

 2024-05-02 109
2024-05-02 109 -
20221028_医疗器械生产现场核查缺陷分析交流(江苏药省监局审核查验中心) (1)VIP免费

 2024-05-09 73
2024-05-09 73 -
医疗器械网络安全漏洞自评报告VIP专享

 2024-11-18 260
2024-11-18 260 -
内审检查表 MDR法规VIP免费

 2025-04-07 152
2025-04-07 152 -
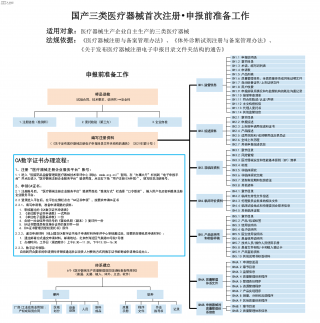
国产三类医疗器械首次注册-申报前准备工作VIP免费
 2025-09-03 18
2025-09-03 18 -
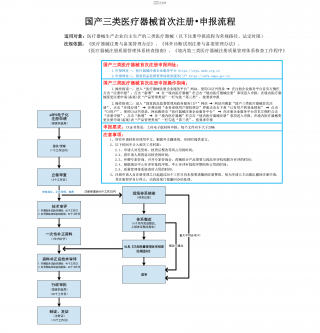
国产三类医疗器械首次注册-申报流程VIP免费
 2025-09-03 23
2025-09-03 23 -
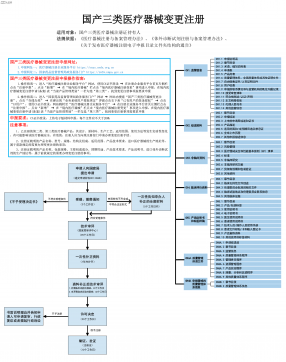
国产三类医疗器械变更注册VIP免费
 2025-09-03 18
2025-09-03 18
作者:多多猪
分类:培训考试
属性:75 页
大小:416.02KB
格式:PDF
时间:2025-08-28


